Lý thuyết chung về flo - brom - iot
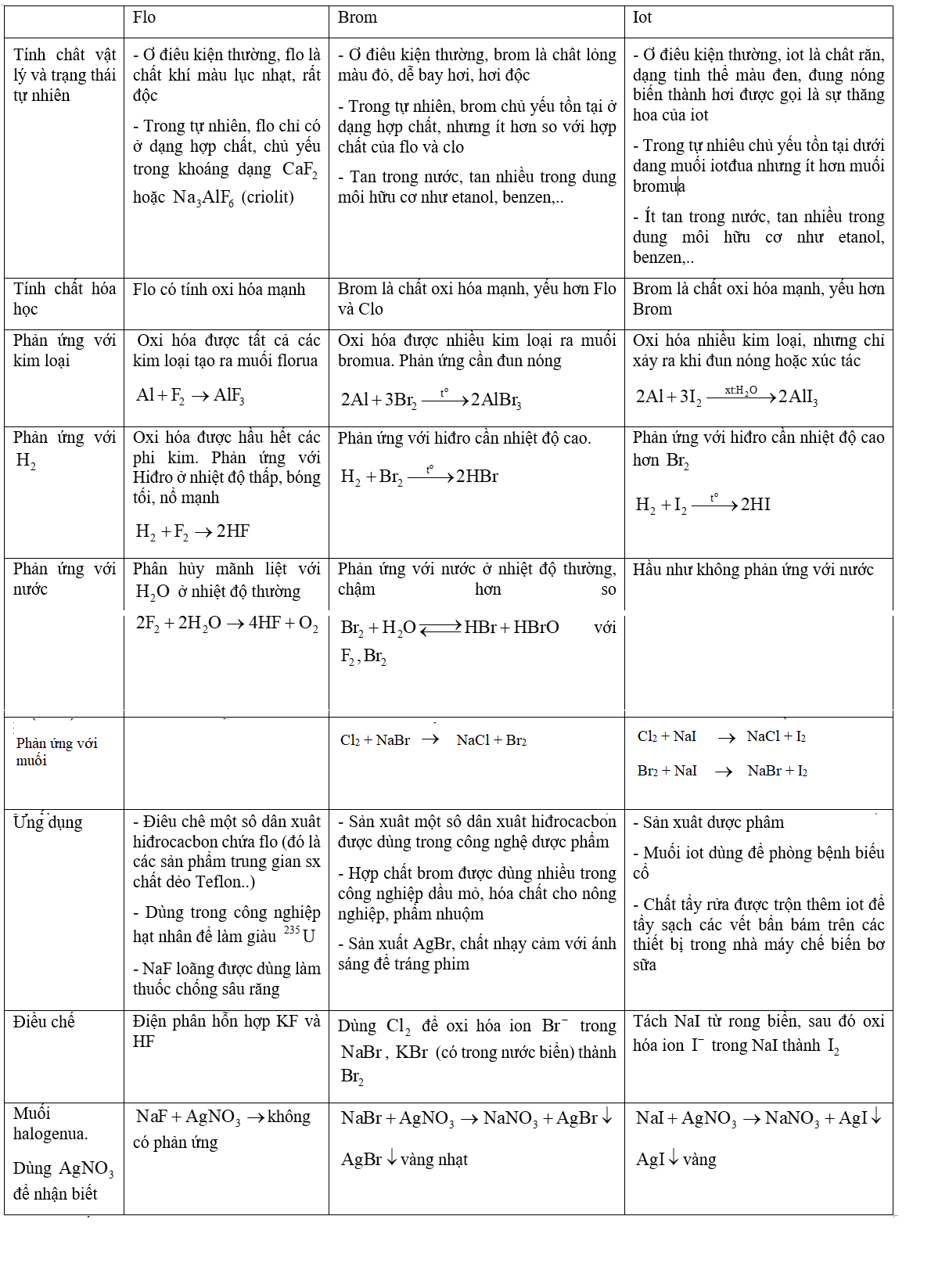
Lý thuyết về Lý thuyết chung về flo - brom - iot
Bài tập tự luyện có đáp án
Câu 1: Dung dịch axit nào sau đây không thể chứa trong bình thủy tinh
- A
- B
- C
- D
Dung dịch $HF$.không thể chứa trong bình thủy tinh do $ 4HF+Si{{O}_{2}}\to Si{{F}_{4}}+2{{H}_{2}}O $
Câu 2: Phát biểu nào sau đây là không đúng?
- A
- B
- C
- D
HF có tính axit yếu hơn HCl
Câu 3: Phản ứng được dùng để điều chế $ B{{r}_{2}} $ trong công nghiệp là
- A
- B
- C
- D
Phản ứng được dùng để điều chế $ B{{r}_{2}} $ trong công nghiệp là : $ 2NaBr+C{{l}_{2}}\to 2NaCl+B{{r}_{2}} $
Câu 4: Phát biểu nào sau đây là không đúng?
- A
- B
- C
- D
Brom chỉ oxi hóa được hiđro ở nhiệt độ cao, tạo khí hiđro bromua
$ {{H}_{2}}+B{{r}_{2}}\xrightarrow{{{t}^{o}}}2HBr $
Câu 5: Nguồn chủ yếu để điều chế brom trong công nghiệp là
- A
- B
- C
- D
Nguồn chủ yếu để điều chế brom trong công nghiệp là nước biển.
Câu 6: Phát biểu nào sau đây là đúng?
- A
- B
- C
- D
- do Flo chỉ có 1 số oxi hóa duy nhất là -1 nên trong các phản ứng hóa học, flo chỉ thể hiện tính oxi hóa
- Các đơn chất halogen $ {{F}_{2}},C{{l}_{2}},B{{r}_{2}},{{I}_{2}} $ đều oxi hoá được nước SAI vì chỉ có flo oxi hóa được nước
- Flo có tính oxi hoá mạnh nhất trong các phi kim nên oxi hoá được tất cả các kim loại; - Tất cả các halogen đều có đồng vị bền trong tự nhiên SAI vì atatin không có đồng vị bền trong tự nhiên
Câu 7: Phản ứng điều chế brom trong công nghiệp là:
- A
- B
- C
- D
Phản ứng điều chế brom trong công nghiệp là: $ 2NaBr+C{{l}_{2}}\to 2NaCl+B{{r}_{2}}. $
Câu 8: Phản ứng nào sau đây là không xảy ra?
- A
- B
- C
- D
Iot không phản ứng với nước
Câu 9: Phản ứng nào sau đây brom chỉ thể hiện tính khử?
- A
- B
- C
- D
$ {{\overset{0}{\mathop{Br}}\,}_{2}}+5{{\overset{0}{\mathop{Cl}}\,}_{2}}+6{{H}_{2}}O\to 10H\overset{-1}{\mathop{Cl}}\,+2H\overset{+5}{\mathop{Br}}\,{{O}_{3}}.$
Câu 10: Nguồn chủ yếu để điều chế iot trong công nghiệp là
- A
- B
- C
- D
Nguồn chủ yếu để điều chế iot trong công nghiệp là rong biển
Câu 11: Hỗn hợp khí nào sau đây không tồn tại ở nhiệt độ thường ?
- A
- B
- C
- D
Phản ứng của hỗn hợp $ {{H}_{2}} $ và $ {{F}_{2}} $ xảy ra ngay ở trong bóng tối và nhiệt độ thấp
$ {{H}_{2}}+{{F}_{2}}\to 2HF $
Câu 12: Dung dịch AgNO3 không phản ứng với dung dịch nào sau đây?
- A
- B
- C
- D
Dung dịch AgNO3 không phản ứng với dung dịch \[ Ca{{F}_{2}} \] vì không tạo kết tủa.
Câu 13: Phản ứng nào sau đây chứng minh tính ăn mòn thủy tinh của axit flohiđric?
- A
- B
- C
- D
Phản ứng chứng minh tính ăn mòn thủy tinh của axit flohiđric: $ Si{{O}_{2}}+4HF\to Si{{F}_{4}}+2{{H}_{2}}O $
Câu 14: Phát biểu nào sau đây không đúng?
- A
- B
- C
- D
Flo oxi hóa được tất cả các kim loại
Câu 15: Phản ứng nào dưới đây không thể xảy ra ?
- A
- B
- C
- D
$ {{I}_{2}} $ có tính oxi hóa yếu hơn $ B{{r}_{2}} $ → Không đẩy được ion Br- ra khỏi dung dịch muối.
Câu 16: Phương pháp nào dưới đây được dùng để điều chế khí $ {{F}_{2}} $ trong công nghiệp ?
- A
- B
- C
- D
Để điều chế $ {{F}_{2}} $ trong công nghiệp, người ta điện phân nóng chảy hỗn hợp KF và HF, hỗn hợp đó ở thể lỏng
Câu 17: Phát biểu nào sau đây không đúng?
- A
- B
- C
- D
Trong hợp chất, flo chỉ có số oxi hóa -1
Câu 18: Phát biểu nào sau đây không đúng?
- A
- B
- C
- D
Phản ứng của flo với hiđro xảy ra ngay trong bóng tối và ở nhiệt độ thường
Câu 19: Axit nào sau đây được dùng để khắc chữ lên thủy tinh?
- A
- B
- C
- D
$ HF $ có tính chất ăn mòn các đồ vật bằng thủy tinh nên được dùng để khắc chữ lên thủy tinh.
Câu 20: Cho phản ứng: $ {{H}_{2}}S+4B{{r}_{2}}+4{{H}_{2}}O\to {{H}_{2}}S{{O}_{4}}+8HBr $ Trong phản ứng trên, brom đóng vai trò
Trong phản ứng trên, brom đóng vai trò
- A
- B
- C
- D
$ {{H}_{2}}\overset{-2}{\mathop{S}}\,+4{{\overset{0}{\mathop{Br}}\,}_{2}}+4{{H}_{2}}O\to {{H}_{2}}\overset{+6}{\mathop{S}}\,{{O}_{4}}+8H\overset{-1}{\mathop{Br}}\, $
Câu 21: Đổ dung dịch $ AgN{{O}_{3}} $ vào dung dịch muối nào sau đây sẽ không có phản ứng?
- A
- B
- C
- D
$ AgN{{O}_{3}} $ không phản ứng với $ NaF $
Câu 22: Khí flo không tác dụng trực tiếp với :
- A
- B
- C
- D
Flo không tác dụng trực tiếp với oxi
Câu 23: Bệnh nhân bị bệnh bướu cổ có thể do thiếu nguyên tố nào sau đây?
- A
- B
- C
- D
Bệnh nhận bị bệnh bướu cổ do thiếu nguyên tố iot
Câu 24: Khi đun nóng, iot rắn biến thành hơi, không qua trạng thái lỏng. Hiện tượng này được gọi là
- A
- B
- C
- D
Khi đun nóng, iot rắn biến thành hơi, không qua trạng thái lỏng. Hiện tượng này được gọi là: sự thăng hoa.
Câu 25: Phản ứng nào sau đây không xảy ra?
- A
- B
- C
- D
Iot có tính oxi hóa yếu hơn brom nên không thể đẩy brom ra khỏi muối
Câu 26: Chất nào trong các chất dưới đây có thể nhận biết được bột gạo ?
- A
- B
- C
- D
Tinh bột có cấu trúc xoắn lò xo, có thể hấp phụ được $ {{I}_{2}} $ làm tinh bột chuyển thành màu xanh.
Câu 27: Ở điều kiện phòng thí nghiệm, đơn chất nào sau đây thăng hoa khi đun nóng?
- A
- B
- C
- D
Ở điều kiện phòng thí nghiệm, iot thăng hoa khi đun nóng tức là iot chuyển từ trạng thái rắn thành hơi mà không qua trạng thái lỏng
Câu 28: Chất nào sau đây tác dụng được với $ NaBr $ giải phóng $ B{{r}_{2}} $
- A
- B
- C
- D
- Flo có tính oxi hóa rất mạnh nên khi cho vào dung dịch sẽ oxi hóa nước trước
- Iot có tính oxi hóa yếu hơn brom nên không thể đẩy brom khỏi muối
Chỉ có clo tác dụng được với $ NaBr $ giải phóng $ B{{r}_{2}} $ : $ C{{l}_{2}}+2NaBr\to 2NaCl+B{{r}_{2}} $
Câu 29: Phản ứng nào sau đây chứng minh tính oxi hóa của iot?
- A
- B
- C
- D
$ 2\overset{0}{\mathop{Al}}\,+3{{\overset{-1}{\mathop{I}}\,}_{2}}\xrightarrow{{{H}_{2}}O}2\overset{+3}{\mathop{Al}}\,{{\overset{-1}{\mathop{I}}\,}_{3}} $
Câu 30: Chọn câu trả lời không đúng trong các câu dưới đây?
- A
- B
- C
- D
Flo là chất khí, có màu lục nhạt nên phát biểu không đúng là: "Flo là chất khí, có màu nâu đỏ"
Câu 31: Chọn câu đúng khi nói về flo, clo, brom, iot
- A
- B
- C
- D
$ {{F}_{2}} $ đốt cháy $ {{H}_{2}}O $ ngay ở nhiệt độ thường: $ 2{{F}_{2}}+2{{H}_{2}}O\to 4HF+{{O}_{2}} $
$ C{{l}_{2}},B{{r}_{2}} $ tác dụng được với $ {{H}_{2}}O $ nhưng không oxi hóa $ {{H}_{2}}O $
$ {{I}_{2}} $ hầu như không phản ứng với $ {{H}_{2}}O $ và không oxi hóa được $ {{H}_{2}}O $
Câu 32: Cho sơ đồ: $ {{F}_{2}}\xrightarrow{+X}HF\xrightarrow{+Y}Si{{F}_{4}} $ Các chất X, Y lần lượt là
Các chất X, Y lần lượt là
- A
- B
- C
- D
$ \begin{array}{l} 2{{F}_{2}}+2{{H}_{2}}O\to 4HF+{{O}_{2}} \\ 4HF+Si{{O}_{2}}\to Si{{F}_{4}}+2{{H}_{2}}O \end{array} $
Câu 33: Phản ứng nào sau đây brom vừa có tính oxi hóa, vừa có tính khử ?
- A
- B
- C
- D
$ 2NaOH+{{\overset{0}{\mathop{Br}}\,}_{2}}\to Na\overset{-1}{\mathop{Br}}\,+Na\overset{+1}{\mathop{Br}}\,O+{{H}_{2}}O $
Câu 34: Nguyên tắc điều chế flo là
- A
- B
- C
- D
Do $ {{F}^{-}} $ không bị oxi hóa bởi các chất oxi hóa thông thường nên chỉ có thể dùng dòng điện oxi hóa muối florua để điều chế flo
Câu 35: Theo dãy: $ HF-HCl-HBr-HI $ thì
- A
- B
- C
- D
Dãy các axit HX từ HF đến HI thì tính khử và tính axit tăng dần.
Câu 36: Phản ứng nào sau đây brom chỉ thể hiện tính oxi hóa?
- A
- B
- C
- D
$ {{\overset{0}{\mathop{Br}}\,}_{2}}+2Na\overset{-1}{\mathop{I}}\,\to 2Na\overset{-1}{\mathop{Br}}\,+{{\overset{0}{\mathop{I}}\,}_{2}} $
Câu 37: Phản ứng nào sau đây không đúng?
- A
- B
- C
- D
Clo có tính oxi hóa yếu hơn flo nên không thể oxi hóa flo từ -1 lên 0.
Câu 38: Số oxi hóa của brom trong các hợp chất $ HBr,HBrO,KBr{{O}_{3}},Br{{F}_{3}} $ lần lượt là:
- A
- B
- C
- D
$ H\overset{-1}{\mathop{Br}}\,,H\overset{+1}{\mathop{Br}}\,O,K\overset{+5}{\mathop{Br}}\,{{O}_{3}},\overset{+3}{\mathop{Br}}\,{{F}_{3}} $
Câu 39: Thuốc thử để nhận ra iot là:
- A
- B
- C
- D
Thuốc thử để nhận ra iot là hồ tinh bột do tạo thành hợp chất màu xanh đặc trưng
Câu 40: Chất nào sau đây chỉ có tính oxi hoá, không có tính khử ?
- A
- B
- C
- D
Flo là phi kim mạnh nhất, chỉ thể hiện tính oxi hóa không có tính khử.
Câu 41: Phản ứng nào sau đây không đúng?
- A
- B
- C
- D
Phản ứng của iot với hiđro là phản ứng thuận nghịch
Câu 42: Để sản xuất $ {{F}_{2}} $ trong công nghiệp, người ta điện phân hỗn hợp :
- A
- B
- C
- D
Để sản xuất $ {{F}_{2}} $ trong công nghiệp, người ta điện phân hỗn hợp : $ KF+2HF $ nóng chảy.
Câu 43: Nhận định nào sau đây không đúng khi nói về flo?
- A
- B
- C
- D
Nhận định không đúng là: flo Có nhiều đồng vị bền trong tự nhiên
Câu 44: Phát biểu nào sau đây đúng?
- A
- B
- C
- D
Iot có độ âm điện nhỏ hơn brom là phát biểu đúng
Câu 45: Phát biểu nào sau đây là không đúng?
- A
- B
- C
- D
Phản ứng của iot với hiđro là phản ứng thuận nghịch; iot chỉ oxi hóa được hiđro ở nhiệt độ cao và có mặt xúc tác
$ {{H}_{2}}+{{I}_{2}}\overset{xt:Pt,{{t}^{o}}}{\leftrightarrows}2HI $
Câu 46: Muối nào sau đây tan được trong nước?
- A
- B
- C
- D
Muối tan được trong nước là AgF.