Đun nóng hỗn hợp hai ancol đơn chức, mạch hở với $\Large\ H_2SO_4$ đặc

MỤC LỤC
Câu hỏi:
Đun nóng hỗn hợp hai ancol đơn chức, mạch hở với $\Large\ H_2SO_4$ đặc, thu được hỗn hợp gồm các ete. Lấy 7,2 gam một trong các ete đó đem đốt cháy hoàn toàn, thu được 8,96 lít khí $\Large\ CO_2$ (ở đktc) và 7,2 gam $\Large\ H_2O$. Hai ancol đó là :
Đáp án án đúng là: D
Lời giải chi tiết:
Đốt cháy ete thu được $\Large\ {{n}_{C{{O}_{2}}}}={{n}_{{{H}_{2}}O}}=0,4$ mol nên suy ra ete có công thức phân tử là $\Large\ C_nH_{2n}O$ (ete không no đơn chức, phân tử có 1 liên kết đôi C=C). Vậy đáp án chỉ có thể là A hoặc D.
Phương trình phản ứng :
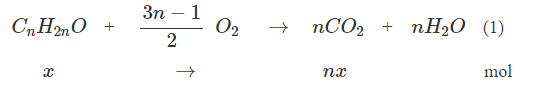
Theo phương trình (1) và giả thiết ta có hệ :
$\Large\ \left\{ \begin{align}
& (14n+16)x=7,2 \\
& nx=0,4 \\
\end{align} \right.$ $\Large\ \Rightarrow \left\{ \begin{align}
& x=0,1 \\
& n=4 \\
\end{align} \right.$
Căn cứ vào các phương án, hai ancol là $\Large\ CH_3OH$ và $\Large\ CH_2=CHCH_2OH$
Xem thêm các bài tiếp theo bên dưới
- X là hợp chất có công thức phân tử $\Large\ C_7H_8O_2$. X tác d
- Một hợp chất X chứa ba nguyên tố C, H, O có tỉ lệ khối lượng $\Large\
- Hỗn hợp Z gồm 1 ancol no mạch hở 2 chức X và 1 ancol no đơn chức mạch
- Đốt cháy hoàn toàn m gam ancol X, sản phẩm thu được cho đi qua bình đự
- Oxi hóa 11,7 gam hỗn hợp E gồm 2 ancol bậc một X và Y (đều no, đơn chứ