Một số muối quan trọng
Lý thuyết về Một số muối quan trọng
MỘT SỐ MUỐI QUAN TRỌNG
I. Natri clorua
1. Trạng thái tự nhiên – cách khai thác
- Natri clorua là thành phần chính của nước biển. Ngoài ra trong lòng đất một lượng lớn NaCl, được gọi là muối mỏ
- Ở những nơi có nước biển hoặc hồ nước măn, người ta khai thác NaCl từ nước mặn ở trên. Cho nước mặn từ từ bay hơi thu được muối kết tinh
- Ở những nơi có muối mỏ, người ta khái thác muối bằng cách đào hầm hoặc giếng sâu qua các lớp đất đá đến muối mỏ. Muối mỏ sau khi khái thác, được nghiền nhỏ và tinh chế để có muối sạch
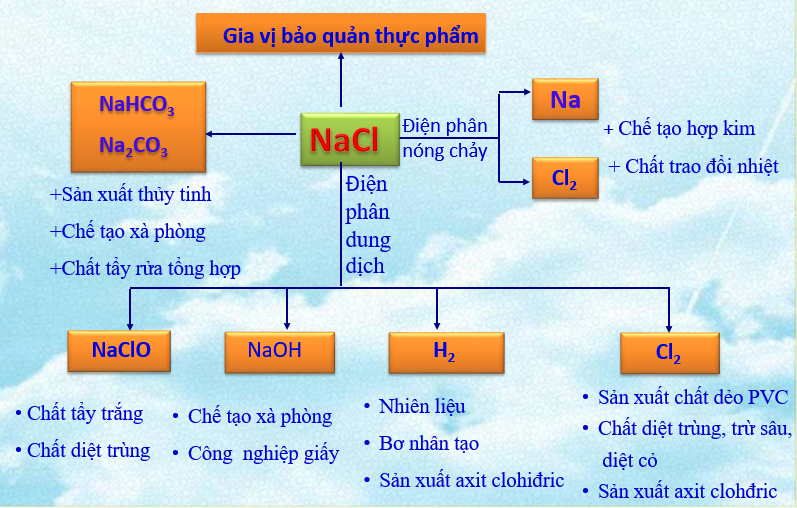
2. Ứng dụng
Muối NaCl có nhiều ứng dụng trong đời sống và sản xuất
II. Muối kali nitrat ( $KN{{O}_{3}}$ )
Muối kali nitrat còn có tên là diêm tiêu, là chất rắn màu trắng. Trong tự nhiên chỉ có một lượng nhỏ kali nitrat
1. Tính chất
- Muối kali nitrat tan nhiều trong nước
- Muối kali nitrat bị phân hủy ở nhiệt độ cao, tạo thành muối kali nitrit và giải phóng khí oxi vì vậy nó có tính chất oxi hóa mạnh
$2KN{{O}_{3}}\xrightarrow{{{t}^{o}}}2KN{{O}_{2}}+{{O}_{2}}$
2. Ứng dụng
Muối kali nitrat được dùng để:
- Chế tạo thuốc nổ đen
- Làm phân bón, cung cấp nguyên tố nitơ và kali cho cây trồng
- Bảo quản thực phẩm trong công nghiệp
Bài tập tự luyện có đáp án
Câu 1: Cho nước biển bay hơi thu được chất rắn là hỗn hợp của nhiều muối. Thành phần chính của hỗn hợp đó là
- A
- B
- C
- D
Thành phần chính của hỗn hợp là $ NaCl $
Câu 2: Ứng dụng nào dưới đây không phải của NaCl?
- A
- B
- C
- D
Ứng dụng không phải của NaCl là chế tạo thuốc nổ
Câu 3: Muối nào dưới đây không tan trong nước?
- A
- B
- C
- D
Muối không tan trong nước là $ BaS{{O}_{4}} $
Câu 4: Công thức hóa học của diêm tiêu là
- A
- B
- C
- D
Công thức hóa học của diêm tiêu là $ KN{{O}_{3}} $
Câu 5: Công thức phân tử của muối natri clorua là
- A
- B
- C
- D
Công thức phân tử của muối natri clorua là $ NaCl $
Câu 6: Phản ứng nào dưới đây đúng?
- A
- B
- C
- D
Phản ứng đúng là :
$ 2KN{{O}_{3\,(r)}}\xrightarrow{{{t}^{o}}}2KN{{O}_{2}}_{\,(r)}+{{O}_{2\,(k)}} $
Câu 7: Muối nào dưới đây tan trong nước?
- A
- B
- C
- D
Muối tan trong nước là $ NaCl $
Câu 8: Tên gọi của muối $ KN{{O}_{3}} $ là
- A
- B
- C
- D
$ KN{{O}_{3}} $ : Kali nitrat
Câu 9: Muối nào dưới đây không tan trong nước, nhưng bị phân hủy ở nhiệt độ cao ?
- A
- B
- C
- D
$ CaC{{O}_{3}} $ không tan trong nước và bị phân hủy ở nhiệt độ cao
$ CaC{{\text{O}}_{3}}\xrightarrow{{{t}^{o}}}CaO+C{{O}_{2}} $
Câu 10: Ứng dụng nào dưới đây là của muối kali nitrat?
- A
- B
- C
- D
Ứng dụng của muối kali nitrat là chế tạo thuốc nổ đen