Một số hợp chất của crom
Lưu về Facebook:
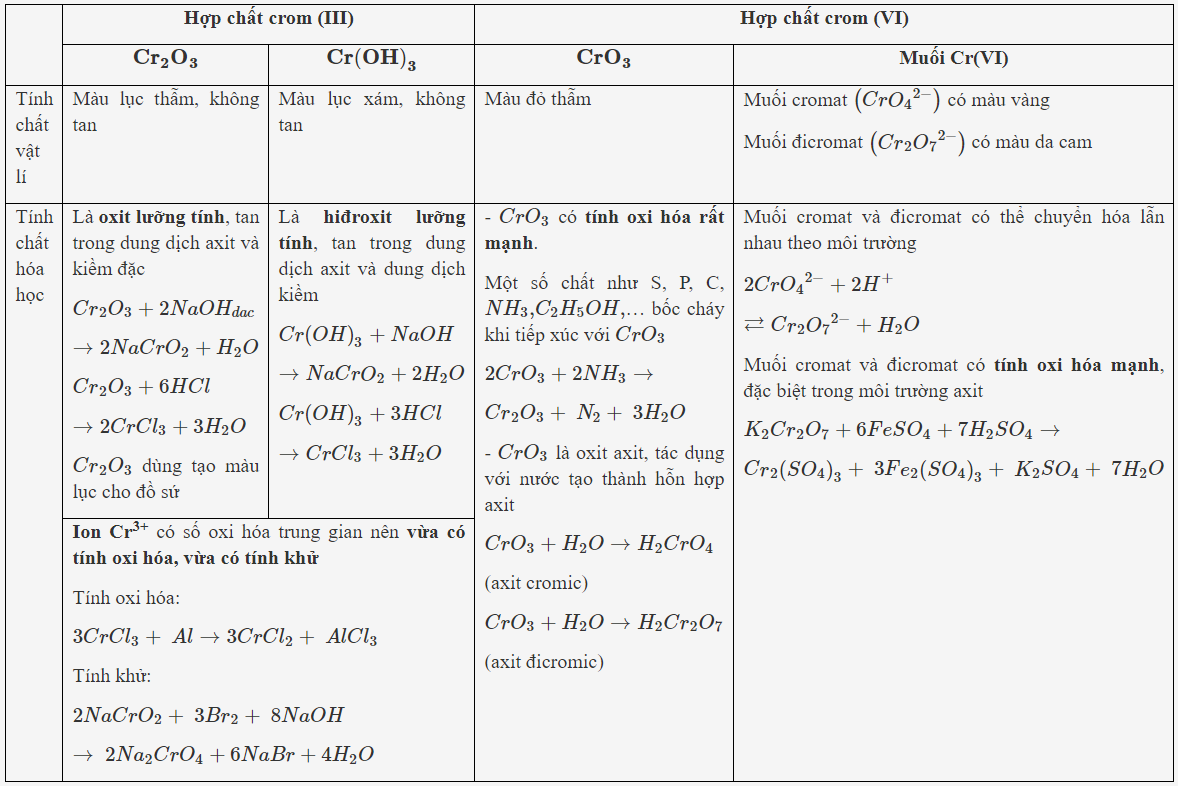
Lý thuyết về Một số hợp chất của crom
Một số hợp chất của crom
Bài tập tự luyện có đáp án
Câu 1: Crom có số oxi hóa +6 trong hợp chất nào sau đây?
- A
- B
- C
- D
Crom có số oxi hóa +6 trong hợp chất $ {{K}_{2}}C{{r}_{2}}{{O}_{7}}. $
Câu 2: Ion nào nào sau đây vừa có tính khử vừa có tính oxi hóa?
- A
- B
- C
- D
Ion vừa có tính oxi hóa vừa có tính khử $ C{{r}^{3+}} $ là số oxi hóa trung gian vừa có thể lên +6 và xuống +2, 0
Câu 3: Crom(VI) oxit là oxit
- A
- B
- C
- D
$ Cr{ O _ 3 } $ thể hiện tính oxi hóa
Câu 4: Chất nào sau đây không có tính lưỡng tính?
- A
- B
- C
- D
Chất lưỡng tính thường gặp: $ C{{r}_{2}}{{O}_{3}},Cr{{\left( OH \right)}_{3}},A{{l}_{2}}{{O}_{3}},Zn{{\left( OH \right)}_{2}}... $
Còn $ Cr{{\left( OH \right)}_{2}} $ không phải lưỡng tính
Câu 5: Dung dịch \[HCl,\] $ {{H}_{2}}S{{O}_{4}} $ loãng phản ứng với \[CrO\] tạo muối
- A
- B
- C
- D
Phương trình phản ứng : $ CrO+2HCl $ $ \xrightarrow{{}} $ $ CrC{{l}_{2}}+{{H}_{2}}O $
Số oxi hóa của \[CrO\] khi phản ứng với \[HCl,\] $ {{H}_{2}}S{{O}_{4}} $ là +2
Câu 6: Trong phản ứng: \[C{r_2}{O_7}^{2 - } + S{O_3}^{2 - } + {H^ + } \to C{r^{3 + }} + X + {H_2}O.\] X là
- A
- B
- C
- D
Phương trình phản ứng: $ C{{r}_{2}}{{O}_{7}}^{2-}+3S{{O}_{3}}^{2-}+8{{H}^{+}} $ $ \xrightarrow{{}} $ $ 2C{{r}^{3+}}+3S{{O}_{4}}^{2-}+4{{H}_{2}}O $