HỢP CHẤT CỦA SẮT
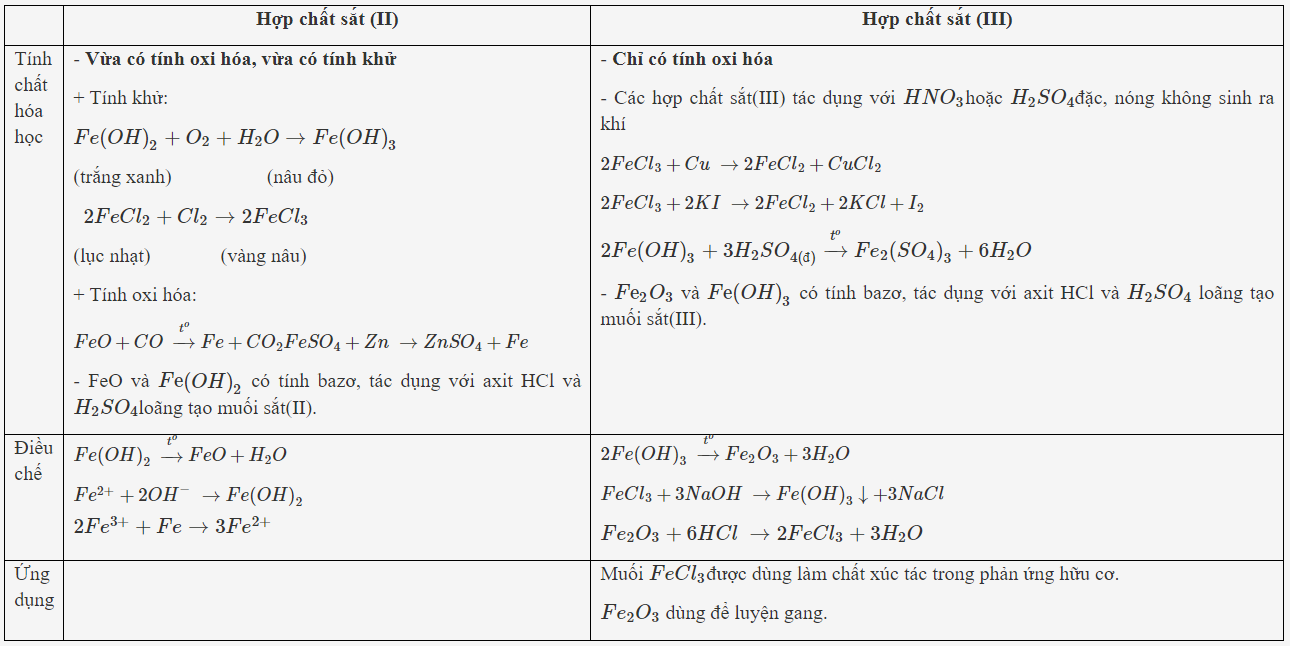
Lý thuyết về HỢP CHẤT CỦA SẮT
HỢP CHẤT CỦA SẮT
Bài tập tự luyện có đáp án
Câu 1: Công thức của sắt(III) oxit là
- A
- B
- C
- D
Công thức của sắt(III) oxit là
Câu 2: Hợp chất sắt(II) nitrat có công thức là
- A
- B
- C
- D
Hợp chất sắt(II) nitrat có công thức là
Câu 3: Kim loại nào sau đây không tác dụng với dung dịch
- A
- B
- C
- D
Ag không tác dụng với dung dịch
Câu 4: Cách bảo quản muối sắt (II) không bị oxi hóa là
- A
- B
- C
- D
Cho thêm một đinh sắt để muối sắt (II) không bị oxi hóa:
Câu 5: Cho dư vào dung dịch chất nào sau đây, thu được kết tủa?
- A
- B
- C
- D
Chất tác dụng với dư thu được kết tủa là Vì các chất còn lại đều tạo phức tan.
Câu 6: Khi thêm dung dịch vào dung dịch sẽ có hiện tượng gì xảy ra?
- A
- B
- C
- D
Phương trình phản ứng:
Câu 7: Nung Fe(NO3)2 trong bình kín, không có không khí, thu được sản phẩm gồm
- A
- B
- C
- D
.
Câu 8: Tính chất hóa học chung của muối sắt (III) là tính
- A
- B
- C
- D
Sắt (III) có số oxi hóa cao nhất của sắt nên chỉ có tính oxi hóa
Câu 9: Công thức của sắt (III) nitrat là
- A
- B
- C
- D
Công thức của sắt (III) nitrat là: .
Câu 10: Tính chất hóa học chung của muối sắt (II) là tính
- A
- B
- C
- D
; có cả tính oxi hóa và tính khử
Câu 11: Chất nào sau đây tác dụng với dung dịch NaOH tạo ra kết tủa màu trắng hơi xanh, dễ hoá nâu trong không khí?
- A
- B
- C
- D
Câu 12: Thành phần chính của quặng pirit là
- A
- B
- C
- D
Thành phần chính của quặng pirit là
Câu 13: Nung , FeO và ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn. Thành phần của chất rắn gồm
- A
- B
- C
- D
Vậy chất rắn gồm .
Câu 14: Sắt (II) oxit là chất rắn màu đen. Công thức của sắt(II) oxit là
- A
- B
- C
- D
Công thức của sắt(II) oxit là
Câu 15: Dung dịch KOH tác dụng với chất nào sau đây tạo ra kết tủa
- A
- B
- C
- D
Câu 16: Nhiệt phân hoàn toàn trong không khi đến khối lượng không đổi, thu được chất rắn là
- A
- B
- C
- D
Câu 17: Chất nào sau đây khi cho tác dụng với đặc, nóng không có khí thoát ra?
- A
- B
- C
- D
khi cho tác dụng với đặc, nóng không có khí thoát ra.
Câu 18: Công thức của sắt(III) hiđroxit là
- A
- B
- C
- D
Công thức của sắt(III) hiđroxit là
Câu 19: Hợp chất FeS có tên gọi
- A
- B
- C
- D
Hợp chất FeS có tên gọi: Sắt (II) sunfua.
Câu 20: Dung dịch không phản ứng với chất nào sau đây?
- A
- B
- C
- D
Dung dịch không phản ứng với Ag.
Câu 21: Công thức hóa học của sắt (III) nitrat là
- A
- B
- C
- D
Công thức hóa học của sắt (III) nitrat là
Câu 22: Công thức phân tử của sắt (III) oxit là
- A
- B
- C
- D
Công thức phân tử của sắt (III) oxit là
Câu 23: Trong các hợp chất của sắt sau đây: FeS, , hợp chất nào có hàm lượng sắt lớn nhất?
- A
- B
- C
- D
Hàm lượng của Fe trong FeO là lớn nhất .
Câu 24: Nhiệt phân trong không khí đến khối lượng không đổi, thu được chất rắn là
- A
- B
- C
- D
Nhiệt phân trong không khí đến khối lượng không đổi, thu được chất rắn là
Câu 25: Cho dung dịch tác dụng với dung dịch NaOH tạo thành kết tủa có màu
- A
- B
- C
- D
Kết tủa màu nâu đỏ.
Câu 26: Chất nào sau đây khi cho tác dụng với đặc, nóng không có khí thoát ra?
- A
- B
- C
- D
khi cho tác dụng với đặc, nóng không có khí thoát ra.
Câu 27: Cho dãy các kim loại sau: Cu, Ni, Zn, Mg, Ba, Ag. Số kim loại trong dãy phản ứng được với dung dịch là
- A
- B
- C
- D
Do tính khử nên Ag không phản ứng với
các kim loại Cu, Ni, Zn, Mg đều khử được .
Ba tạo kết tủa với dd .
Vậy só kim loại trong dãy phản ứng được với dung dịch là 5.
Câu 28: Điều chế ta có thể dùng cách nào sau đây?
- A
- B
- C
- D
Điều chế muối sắt (II) clorua ta có thể dùng sắt khử muối sắt (III) clorua:
Câu 29: Quặng manhetit là quặng giàu sắt nhất nhưng hiếm có trong tự nhiên. Trong quặng manhetit chứa nhiều hợp chất sắt nào sau đây?
- A
- B
- C
- D
Trong quặng manhetit chứa
Câu 30: Công thức của oxit sắt từ là
- A
- B
- C
- D
Công thức của oxit sắt từ là
Câu 31: Tính chất hóa học đặc trưng của hợp chất sắt (II) là
- A
- B
- C
- D
Tính chất hóa học đặc trưng của hợp chất sắt (II) là tính khử.
Xem thêm các bài tiếp theo bên dưới