Hỗn hợp Z gồm 1 ancol no mạch hở 2 chức X và 1 ancol no đơn chức mạch

MỤC LỤC
Câu hỏi:
Hỗn hợp Z gồm 1 ancol no mạch hở 2 chức X và 1 ancol no đơn chức mạch hở Y (các nhóm chức đều bậc 1) có tỉ lệ số mol $\Large\ n_X : n_Y = 1 : 3$. Cho m gam hỗn hợp Z tác dụng với natri dư thu được 6,72 lít $\Large\ H_2$ (đktc). Mặt khác cho m gam hỗn hợp Z tác dụng với $\Large\ CuO$ dư đun nóng sau khi phản ứng kết thúc thu được 38,64 gam hỗn hợp andehit và hơi nước. Để đốt cháy m gam hỗn hợp Z cần bao nhiêu lít $\Large\ O_2$ (đktc) ?
Đáp án án đúng là: A
Lời giải chi tiết:
Gọi CTPT X là $\Large\ R(CH_2OH)_2$ và CTPT Y là $\Large\ R^,CH_2OH$
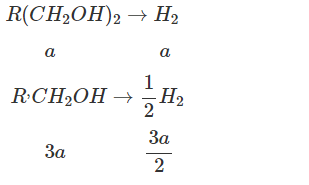
$\Large\Rightarrow \ \sum n_{H_2} = a + \dfrac{3a}{2} = 0,3 \Rightarrow a= 0,12$ mol
Mặt khác, xét phản ứng oxi hóa hh Z:
$\Large\ R(CH_2OH)_2 + 2CuO \overset{t^o}{\rightarrow} R(CHO)_2 + 2Cu + 2H_2O$
$\Large\ R^,CH_2OH + CuO \to R^,CHO + Cu + H_2O$
=> $\Large\ m_{andehit} + m_{H_2O} = m_{ancol} + m_{O(CuO)}$
=> $\Large\ m_{ancol} = 38,64 - 0,6.16 = 29,04$ g
Đốt cháy anđehit thì cần khối lượng $\Large\ O_2$ đúng bằng lượng $\Large\ O_2$ để đốt cháy ancol
X: $\Large\ C_nH_{2n+2}O_2 + ( \dfrac{3n - 1}{2}) O_2 \to nCO_2 + (n+1) H_2O$
Y: $\Large\ C_mH_{2m+2}O + ( \dfrac{3m}{2}) O_2 \to mCO_2 + (m+1) H_2O$
Có $\Large\ m_{ancol} = 0,12(14n + 34) + 0,36(14m+18) = 29,04$
$\Large\ \Leftrightarrow 1,68n +5,04m = 18,48$ (g) (1)
$\Large\ m_{O_2} = 0,12.\dfrac{3n - 1}{2}.32 + 0,36.\dfrac{3m}{2}.32 = 5,76n + 17,28m - 1,92$ (2)
Từ (1) $\Large\Rightarrow 5,76n + 17,28m = 63,36$, thay vào (2)
$\Large\Rightarrow m_{O_2} = 61,44 \Rightarrow n_{O_2} = 1,92$ mol
$\Large\Rightarrow V_{O_2} = 1,92. 22,4 = 43,008$ lít
Xem thêm các bài tiếp theo bên dưới
- Đốt cháy hoàn toàn m gam ancol X, sản phẩm thu được cho đi qua bình đự
- Oxi hóa 11,7 gam hỗn hợp E gồm 2 ancol bậc một X và Y (đều no, đơn chứ
- Anđehit axetic (etanal) có công thức là: A. $\Large HCHO$. B. $\Large
- Cho 21,6 gam hỗn hợp gồm rượu etylic, axit fomic và etylenglicol tác d
- Tên gọi của $\Large C_{6}H_{5}CHO$ (chứa vòng benzen) là: A. anđehit o