Hòa tan hoàn toàn m gam hỗn hợp $\Large X$ gồm $\Large Ba$, $\Large Ba
MỤC LỤC
Câu hỏi:
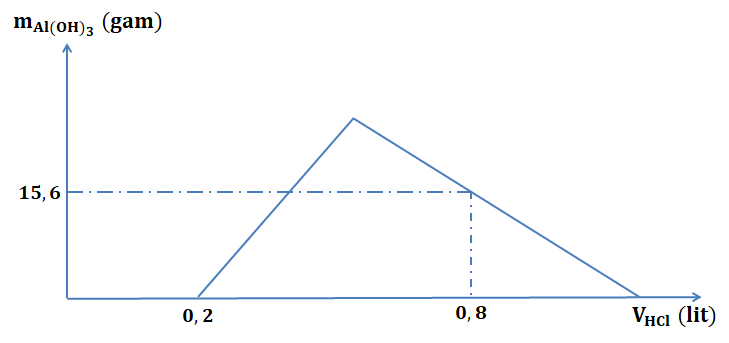
Hòa tan hoàn toàn m gam hỗn hợp $\Large X$ gồm $\Large Ba$, $\Large BaO$, $\Large Al$ và $\Large Al_{2}O_{3}$ vào nước dư, thu được dung dịch $\Large Y$ và 5,6 lít $\Large H_{2}$ (đktc). Nhỏ từ từ đến dư dung dịch $\Large HCl$ 1M vào dung dịch $\Large Y$. Đồ thị biểu diễn sự phụ thuộc khối lượng kết tủa $\Large Al(OH)_{3}$ theo thể tích dung dịch $\Large HCl$ 1M như sau:

Giá trị của m là:
Đáp án án đúng là: C
Lời giải chi tiết:
Đáp án C
Theo đồ thị thì kết tủa xuất hiện khi $\Large n_{H^{+}} = 0,2$.
$\Large \Rightarrow n_{OH^{-}} = 0,2$
Khi $\Large n_{H^{+}} = 0,8$ thì kết tủa bị hòa tan một phần và còn lại 0,2 mol $\Large Al(OH)_{3}$
$\Large \Rightarrow n_{H^{+}}= n_{OH^{-}} + 4n_{AlO_{2}^{-}} - 3n_{Al(OH)_{3}}$
$\Large \Rightarrow n_{OH^{-}} = 0,3$
Bảo toàn điện tích cho Y
$\Large \Rightarrow n_{Ba^{2+}}=\dfrac{n_{OH^{-}}+n_{OH^{-}}}{2}= 0,25$
Bảo toàn kim loại
$\Large \Rightarrow$ X chứa $\Large Al$ (0,3), $\Large Ba$ (0,25) và $\Large O$
Bảo toàn electron
$\Large \Rightarrow 3n_{Al} + 2n_{Ba} = 2n_{O} + 2n_{H_{2}}$
$\Large \Rightarrow n_{O} = 0,45$
$\Large \Rightarrow m_{X} = 49,55$
Xem thêm các bài tiếp theo bên dưới
- Ở điều kiện thường hợp chất nào sau đây tác dụng được với nước A. $\La
- Trước khi thi đấu các môn thể thao, các vận động viên thường xoa một í
- Trộn kim loại X với bột sắt oxit (gọi hỗn hợp tecmit) để thực hiện phả
- Thành phần chính của quặng photphorit là: A. $\Large CaHPO_{3}$ B. $\L
- Cho các kim loại sau: $\Large Li$, $\Large Na$, $\Large Al$, $\Large C