Cho m gam một ancol (rượu) no, đơn chức X qua bình đựng $\Large\ CuO$

MỤC LỤC
Câu hỏi:
Cho m gam một ancol (rượu) no, đơn chức X qua bình đựng $\Large\ CuO$ (dư), nung nóng. Sau khi phản ứng hoàn toàn, khối lượng chất rắn trong bình giảm 0,32 gam. Hỗn hợp hơi thu được có tỉ khối đối với hiđro là 15,5. Giá trị của m là :
Đáp án án đúng là: A
Lời giải chi tiết:
Đặt công thức phân tử của ancol no, đơn chức X là : $\Large\ C_nH_{2n + 2}O$
Phương trình phản ứng :
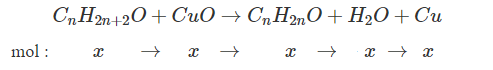
Khối lượng chất rắn giảm = $\Large\ m_{CuO} – m_{Cu} = 80x – 64x = 0,32 \to x = 0,02$
Cách 1 (Áp dụng sơ đồ đường chéo) : Hỗn hợp hơi gồm $\Large\ C_nH_{2n}O$ và $\Large\ H_2O$ có khối lượng mol trung bình là: 15,5.2 = 31 gam/mol.
Áp dụng sơ đồ đường chéo ta có :
$\Large\ \dfrac{{{n}_{{{C}_{n}}{{H}_{2n}}O}}}{{{n}_{{{H}_{2}}O}}}=\dfrac{31-18}{(14n+16)-31}=\dfrac{13}{14n-15}=\dfrac{1}{1}\Rightarrow n=2$
Vậy khối lượng của X là:
$\Large m = (14n + 18).0,02 = (14.2 + 18).0,02 = 0,92$ gam.
Cách 2 (Áp dụng định luật bảo toàn khối lượng): Hỗn hợp hơi gồm $\Large\ C_nH_{2n}O$ và $\Large\ H_2O$ có khối lượng mol trung bình là 15,5.2 = 31 và có số mol là 0,02.2 = 0,04 mol.
Áp dụng định luật bảo toàn khối lượng ta có :
$\Large\ m_{C_nH_{2n+2}O}=0,02.64+0,04.31-0,02.80=0,92$ gam.
Xem thêm các bài tiếp theo bên dưới
- Đốt cháy hoàn toàn 3,2 gam một chất hữu cơ A (C, H, O) dẫn toàn bộ sản
- Hòa tan m gam ancol etylic (D = 0,8 g/ml) vào 108 ml nước (D = 1 g/ml)
- Hỗn hợp X gồm $\Large\ CH_3OH$ và $\Large\ CH_2=CH-CH_2OH$. Cho m gam
- Cho $\Large\ Na$ tác dụng vừa đủ với 1,24 gam hỗn hợp 3 ancol đơn chức
- Tách nước hoàn toàn 16,6 gam hỗn hợp A gồm 2 ancol X,Y ($\Large\ M_X <